Nguyên tử khối là khái niệm quen thuộc trong môn Hóa học. Trong nội dung bài viết này, chúng ta sẽ tìm hiểu chi tiết về bảng nguyên tử khối, bài ca nguyên tử khối và phương pháp nhớ nhanh nhất. Hãy cùng theo dõi nhé!

Nguyên tử khối là gì?
Nguyên tử khối hay khối lượng nguyên tử là khối lượng của một nguyên tử tính bằng đơn vị Cacbon (đvC). Mỗi nguyên tố sẽ có một nguyên tử khối khác nhau.
Như vậy, một nguyên tử bao gồm nhiều thành phần khác nhau (p, e, n) thì khối lượng nguyên tử sẽ bằng tổng các thành phần đó. Tuy nhiên, do khối lượng của e rất nhỏ nên thường được cho bằng 0. Đó là lý do khi nhắc đến khối lượng nguyên tử thì thường là tổng của p và n.
m = mp + mn
Ví dụ: Nguyên tử khối của Mg là 24 đvC, của Zn là 65 đvC
Đơn vị của nguyên tử khối là gì?
Trên thực tế, khối lượng của các nguyên tử vô cùng bé. Bởi vậy, nếu tính bằng gam thì số trị rất nhỏ, không phù hợp để sử dụng.
Ví dụ: Khối lượng của 1 nguyên tử cacbon là 0, 000 000 000 000 000 000 000 019 926 gam (= 1,9926.10-23 gam). Việc này sẽ gây khó khăn trong quá trình tính toán. Bởi vậy, các nhà khoa học đã dùng một cách khác để làm đơn vị của khối lượng của nguyên tử.
Cụ thể, các nhà khoa học đã quy ước lấy 1/12 khối lượng của nguyên tử cacbon làm đơn vị của nguyên tử khối. Đơn vị cacbon, viết tắt là đvC. Trong ký hiệu quốc tế, khối lượng nguyên tử ký hiệu là “u”. Dựa vào đơn vị này, chúng ta có thể dễ dàng tính toán và biểu thị khối lượng của một nguyên tử.
Nguyên tử khối trung bình và công thức tính
Hầu hết các nguyên tố đều tồn tại dưới dạng hỗn hợp của nhiều đồng vị khác nhau với tỉ lệ % nguyên tử được xác định. Khi đó, nguyên tử khối của nguyên tố có nhiều đồng vị là nguyên tử khối trung bình của hỗn hợp các đồng vị tính theo % số nguyên tử tương ứng.
Công thức tính nguyên tử khối trung bình:
M = (x1*M1 + x2*M2 + … + xn*Mn)/100
Trong đó:
- M là nguyên tử khối trung bình
- x1, x2, …, xn là tỉ lệ phần trăm các đồng vị
- M1, M2, …, Mn là nguyên tử khối của các đồng vị
Ví dụ: Nguyên tử A có 2 đồng vị A1 và A2 với tỉ lệ phần trăm lần lượt là x1, x2 thì khối lượng nguyên tử trung bình sẽ là:
A = (x1*A1 + x2*A2)/100
Cách tính khối lượng thực của nguyên tử
Khối lượng tính bằng gam là khối lượng thực của các nguyên tử. Để tính khối lượng nguyên tử thực thì bạn thực hiện theo các bước sau:
- Bước 1: Nắm rõ 1đvC = 0,166.10-26 kg = 0,166.10-23 g
- Bước 2: Dựa vào bảng nguyên tử khối bên trên. Chẳng hạn nguyên tố A có nguyên tử khối là a, tức A = a.
- Bước 3: Khối lượng thực của nguyên tử A là: mA = a * 0,166.10-23 g. Còn khối lượng thực của nguyên tử A là: mA = a * 0,166.10-23 g
Ví dụ: Cho 16g oxy. Xác định nguyên tử oxi có trong 16g oxi và tính khối lượng nguyên tử đó.
Lời giải:
Áp dụng công thức tính nguyên tử khối, ta có:
Số nguyên tử = Khối lượng tính bằng g/Khối lượng tính bằng g của 1 nguyên tử
=> Số nguyên tử trong 16g oxi được xác định là: 16 / (16*0,166.10-23) = 6,02.10-23 gam
1 mol oxi có khối lượng 16g = 16(đvC) thì 1 nguyên tử oxi sẽ có khối lượng là 6,02.10-23 gam
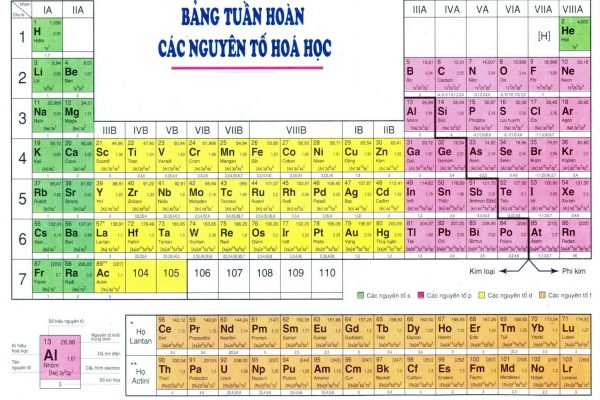
Bảng nguyên tử khối của các nguyên tố
Để thuận lợi cho việc tính toán, bạn có thể tham khảo bảng khối lượng nguyên tử dưới đây.
Bảng nguyên tử khối của đơn chất
|
STT |
Tên nguyên tố |
Ký hiệu |
Nguyên tử khối |
|
1 |
Hiđro |
H |
1 |
|
2 |
Heli |
He |
4 |
|
3 |
Liti |
Li |
7 |
|
4 |
Beri |
Be |
9 |
|
5 |
Bo |
B |
11 |
|
6 |
Cacbon |
C |
12 |
|
7 |
Nitơ |
N |
14 |
|
8 |
Oxi |
O |
16 |
|
9 |
Flo |
F |
19 |
|
10 |
Neon |
Ne |
20 |
|
11 |
Natri |
Na |
23 |
|
12 |
Magie |
Mg |
24 |
|
13 |
Nhôm |
Al |
27 |
|
14 |
Silic |
Si |
28 |
|
15 |
Photpho |
P |
31 |
|
16 |
Lưu huỳnh |
S |
32 |
|
17 |
Clo |
Cl |
35,5 |
|
18 |
Argon |
Ar |
39,9 |
|
19 |
Kali |
K |
39 |
|
20 |
Canxi |
Ca |
40 |
|
21 |
Scandi |
Sc |
44.955912(6) |
|
22 |
Titan |
Ti |
47,867(1) |
|
23 |
Vanadi |
V |
50,9415(1) |
|
24 |
Crom |
Cr |
51,9961(6) |
|
25 |
Mangan |
Mn |
54,938044 |
|
26 |
Sắt |
Fe |
55,845 |
|
27 |
Coban |
Co |
58,933195 |
|
28 |
Niken |
Ni |
58,6934 |
|
29 |
Đồng |
Cu |
63,546 |
|
30 |
Kẽm |
Zn |
65,38 |
|
31 |
Gali |
Ga |
69,723 |
|
32 |
Gecmani |
Ge |
72,64 |
|
33 |
Asen |
As |
74,9216 |
|
34 |
Selen |
Se |
78.96 |
|
35 |
Brom |
Br |
79,904 |
|
36 |
Kryton |
Kr |
83,798 |
|
37 |
Rubidi |
Rb |
85,4678 |
|
38 |
Stronti |
Sr |
87,62 |
|
39 |
Yttri |
Y |
88,90585 |
|
40 |
Zicorni |
Zr |
91,224 |
|
41 |
Niobi |
Nb |
92,90638 |
|
42 |
Molypden |
Mo |
95,95 |
|
43 |
Tecneti |
Tc |
98 |
|
44 |
Rutheni |
Ru |
101,07 |
|
45 |
Rhodi |
Rh |
102,9055 |
|
46 |
Paladi |
Pd |
106,42 |
|
47 |
Bạc |
Ag |
107,8682 |
|
48 |
Cadmi |
Cd |
112,411 |
|
49 |
Indi |
In |
114,818 |
|
50 |
Thiếc |
Sn |
118,71 |
|
51 |
Antimon |
Sb |
121,76 |
|
52 |
Telua |
Te |
127,6 |
|
53 |
I ốt |
I |
126,90447 |
|
54 |
Xenon |
Xe |
131,293 |
|
55 |
Xêsi |
Cs |
132,90545 |
|
56 |
Bari |
Ba |
137,327 |
|
57 |
Lantan |
La |
138,90547 |
|
58 |
Xeri |
Cs |
140,116 |
|
59 |
Praseodymi |
Pr |
140,90765 |
|
60 |
Neodymi |
Nd |
144,242 |
|
61 |
Promethi |
Pm |
145 |
|
62 |
Samari |
Sm |
150,36 |
|
63 |
Europi |
Eu |
151,964 |
|
64 |
Gadolini |
Gd |
157,25 |
|
65 |
Terbi |
Tb |
158,92535 |
|
66 |
Dysprosi |
Dy |
162,5 |
|
67 |
Holmi |
Ho |
164,93032 |
|
68 |
Erbi |
Er |
167,259 |
|
69 |
Thuli |
Tm |
168,93421 |
|
70 |
Ytterbium |
Yb |
173,04 |
|
71 |
Luteti |
Lu |
174,967 |
|
72 |
Hafni |
Hf |
178,49 |
|
73 |
Tantal |
Ta |
180,94788 |
|
74 |
Wolfram |
W |
183,84 |
|
75 |
Rheni |
Re |
186,207 |
|
76 |
Osmi |
Os |
190,23 |
|
77 |
Iridi |
Ir |
192,217 |
|
78 |
Platin |
Pt |
195,084 |
|
79 |
Vàng |
Au |
196,96657 |
|
80 |
Thủy ngân |
Hg |
200,59 |
|
81 |
Tali |
TI |
204,3833 |
|
82 |
Chì |
Pb |
207,2 |
|
83 |
Bitmut |
Bi |
208,9804 |
|
84 |
Poloni |
Po |
209 |
|
85 |
Astatin |
At |
210 |
|
86 |
Radon |
Rn |
222 |
|
87 |
Franxi |
Fr |
223 |
|
88 |
Radi |
Ra |
226 |
|
89 |
Actini |
Ac |
227 |
|
90 |
Thori |
Th |
232,03806 |
|
91 |
Protactini |
Pa |
231,03588 |
|
92 |
Urani |
U |
238,02891 |
|
93 |
Neptuni |
Np |
237,0482 |
|
94 |
Plutoni |
Pu |
244 |
|
95 |
Americi |
Am |
243 |
|
96 |
Curi |
Cm |
247 |
|
97 |
Berkeli |
Bk |
247 |
|
98 |
Californi |
Cf |
251 |
|
99 |
Einsteini |
Es |
252 |
|
100 |
Fermi |
Fm |
257 |
|
101 |
Mendelevi |
Md |
258 |
|
102 |
Nobeli |
No |
259 |
|
103 |
Lawrenci |
Lr |
262 |
|
104 |
Rutherfordi |
Rf |
267 |
|
105 |
Dubni |
Db |
268 |
|
106 |
Seaborgi |
Sg |
[269] |
|
107 |
Bohri |
Bh |
[270] |
|
108 |
Hassi |
Hs |
[269] |
|
109 |
Meitneri |
Mt |
[278] |
|
110 |
Darmstadti |
Ds |
[281] |
|
111 |
Roentgeni |
Rg |
[281] |
|
112 |
Copernixi |
Cn |
[285] |
|
113 |
Nihoni |
Nh |
[286] |
|
114 |
Flerovi |
Fl |
[289] |
|
115 |
Moscovi |
Mc |
[288] |
|
116 |
Livermori |
Lv |
[293] |
|
117 |
Tennessine |
Ts |
[294] |
|
118 |
Oganesson |
Og |
[294] |
Bảng nguyên tử khối của một số nhóm
|
STT |
Tên nhóm |
Công thức hóa học |
Nguyên tử khối |
|
1 |
Hidroxit |
-OH |
17 |
|
2 |
Clorua |
-Cl |
35.5 |
|
3 |
Bromua |
-Br |
80 |
|
4 |
Iotdua |
-I |
127 |
|
5 |
Nitrit |
-NO2 |
46 |
|
6 |
Nitrat |
-NO3 |
62 |
|
7 |
Sunfua |
=S |
32 |
|
8 |
Sunfit |
=SO3 |
80 |
|
9 |
Sunfat |
=SO4 |
96 |
|
10 |
Cacbonat |
=CO3 |
60 |
|
11 |
Photphit |
≡PO3 |
79 |
|
12 |
Photphat |
≡PO4 |
95 |
|
13 |
Hidrophotphat |
=HPO4 |
96 |
|
14 |
Dihidrophotphat |
-H2PO4 |
97 |
|
15 |
Hidrophotphit |
=HPO3 |
80 |
|
16 |
Dihidrophotphit |
-H2PO3 |
81 |
|
17 |
Hidro Sunfat |
-HSO4 |
97 |
|
18 |
Hidrosunfit |
-HSO3 |
81 |
|
19 |
Hidrosunfua |
-HS |
33 |
|
20 |
Hidrocacbonat |
-HCO3 |
61 |
|
21 |
Silicat |
=SiO3 |
76 |
Bài ca nguyên tử khối
Một phương pháp để nhớ bảng khối lượng nguyên tử nhanh chóng và nhớ lâu đó là sử dụng bài ca nguyên tử khối. Dưới đây là bài ca nguyên tử khối mà bạn có thể tham khảo:
Hidro là 1
12 cột Cacbon
Nitơ 14 tròn
Oxi trăng 16
Natri hay láu táu
Nhảy tót lên 23
Khiến Magie gần nhà
Ngậm ngùi nhận 24
27 nhôm la lớn
Lưu huỳnh giành 32
Khác người thật là tài
Clo 35 rưỡi
Kali thích 39
Canxi tiếp 40
55 Mangan cười
Sắt đây rồi 56
64 đồng nổi cáu
vì kém kẽm 65
80 brom nằm
xa bạc 108
Bari thì chán ngán
137 ích chi
Kém người ta còn gì
Thuỷ ngân 201
Còn lại chì một cột
207 thật to
Heli thì buồn so
Mình đây được có 4
Liti thật khiêm tốn
Số 7 là được rồi
Số 9 Beri ngồi
Trêu bạn Bo 11
19 đây chết ngột
Flo đang than phiền
Neon thì cười hiền
Tớ 20 tròn chẵn
Silic người đứng đắn
Nhân 28 đẹp ko
Photpho đỏ hồng hồng
Nhận 31 cuối tháng
Agon cười trong sáng
39,9 đây
Kết thúc bài ca này
Crom 52 đấy

Bài tập về nguyên tử khối
Bài 1: Biết nguyên tử nhôm có 13 proton và 14 nơtron. Khối lượng tính bằng gam của nguyên tử nhôm là bao nhiêu?
A. 5,32.10-23 gam.
B. 6,02.10-23 gam.
C. 4,48.10-23 gam.
D. 3,99.10-23 gam.
Đáp án C
Bài 2: Nguyên tử magie nặng hay nhẹ hơn bao nhiêu lần so với nguyên tử cacbon?
A. 1 lần
B. 2 lần
C. 3 lần
D. 4 lần
Đáp án B
Bài 3: Nguyên tử X nặng gấp 4 lần nguyên tử nitơ. X thuộc nguyên tố nào?
A. Al
B. C
C. Fe
D. Zn
Đáp án C
Bài 4: Khối lượng của một nguyên tử cacbon là 19,9265.10-23 gam. Khối lượng của 1 đvC là bao nhiêu?
A. 8,553. 10-23 gam.
B. 2,6605. 10-23 gam.
C. 0,16605. 10-23 gam.
D. 18,56. 10-23 gam.
Đáp án C
Bài 5: Biết rằng 4 nguyên tử Mg nặng bằng ba nguyên tử của nguyên tố X. Tên của nguyên tố X là:
A. Sắt.
B. Lưu huỳnh.
C. Nitơ.
D. Can xi.
Đáp án C
Bài 6: Khối lượng tương đối của một phân tử H2O là bao nhiêu?
A. 18 đvC.
B. 18 gam.
C. 34 đvC.
D. 18kg.
Đáp án A
Bài 7: Biết nguyên tử nitơ có thành phần gồm có 7 proton, 7 notron và 7 electron. Khối lượng của toàn nguyên tử nitơ là bao nhiêu?
A. 14 gam.
B. 21 gam.
C. 2,34.10-23 gam.
D. 2,34.10-27 gam.
Đáp án C
Bài 8: Một nguyên tử chỉ có 1 electron ở vỏ nguyên tử. Hạt nhân nguyên tử có khối lượng xấp xỉ 3u. Số hạt proton và hạt nơtron trong hạt nhân nguyên tử này lần lượt là
A. 1 và 0.
B. 1 và 2.
C. 1 và 3.
D. 3 và 0.
Đáp án B
Bài 9: Hai nguyên tử Mg nặng gấp mấy lần nguyên tử O?
A. 1.
B. 2.
C. 3.
D. 4.
Đáp án C
Trên đây là những thông tin về nguyên tử khối và bài tập vận dụng. Mong rằng bài viết sẽ giúp bạn hiểu rõ hơn về kiến thức này.