Phản ứng oxi hóa khử là một loại phản ứng rất phổ biến trong lĩnh vực Hóa học. Trong nội dung bài viết này, chúng ta sẽ tìm hiểu chi tiết về cơ chế oxi hóa khử và các bài tập liên quan. Hãy cùng tham khảo nhé!
Phản ứng oxi hóa khử là gì?
Phản ứng oxi hóa khử là loại phản ứng hóa học có sự dịch chuyển electron giữa các chất tham gia phản ứng. Hiểu đơn giản hơn, phản ứng oxi hóa khử làm cho số oxi hóa của một số nguyên tố trong phản ứng thay đổi.

Phản ứng oxi hóa khử gồm có những chất sau:
- Chất khử là các chất nhường electron
- Chất oxy hóa là các chất nhận electron
Trong phản ứng oxi hóa khử sẽ xảy ra các quá trình:
- Quá trình oxi hóa là quá trình nhường electron
- Quá trình khử là quá trình nhận electron
Ví dụ về phản ứng oxi hóa khử:
Fe + CuSO4 → Cu + FeSO4
Quá trình thay đổi số oxi hóa:
Fe0 → Fe2+ + 2e,
Cu2+ + 2e → Cu0
Vai trò của các chất trong phản ứng:
- Sắt là chất khử vì đã nhường electron
- Đồng là chất oxi hóa vì đã nhận 2 electron
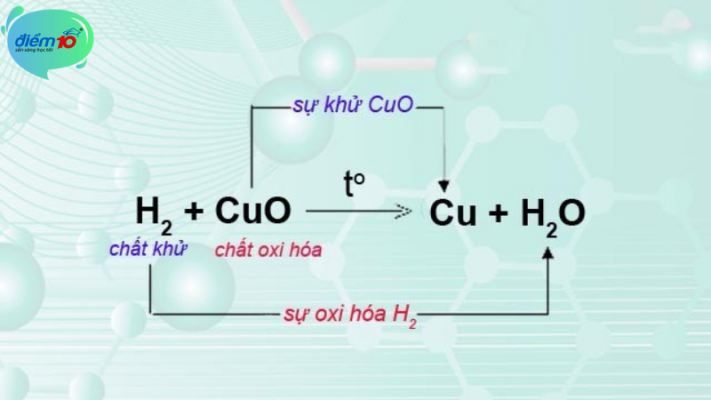
Các bước viết phương trình phản ứng oxi hóa khử chính xác
Để viết phương trình phản ứng oxi hóa khử thì bạn thực hiện theo các bước sau:
- Bước 1: Xác định số oxi hóa của các nguyên tố trong phản ứng để tìm chất oxi hóa và chất khử
- Bước 2: Viết quá trình oxi hóa và quá trình khử sau đó bạn cân bằng mỗi quá trình.
- Bước 3: Tìm hệ số thích hợp cho chất oxi hóa và chất khử sao cho tổng số electron cho bằng tổng số electron nhận.
- Bước 4: Đặt hệ số của các chất oxi hóa và chất khử vào sơ đồ phản ứng. Từ đó bạn tính ra hệ số các chất khác. Kiểm tra cân bằng số nguyên tử của các nguyên tố và cân bằng điện tích hai vế của phương trình hóa học.
Các loại phản ứng oxi hóa khử
Có một số loại phản ứng oxi hóa khử sau:
Phản ứng oxi hóa khử thông thường
Tồn tại chất khử và chất oxi hóa ở 2 phân tử khác nhau
Ví dụ:
Cu + 2H2SO4 đặc → CuSO4 + SO2 + 2H2O
C + 4HNO3 đặc → CO2 + 4NO2 + 2H2O
Phản ứng oxi hóa khử nội phân
Phản ứng mà có chất khử và chất oxi hóa thuộc cùng 1 phân tử nhưng lại ở 2 nguyên tử khác nhau trong phản ứng.
Ví dụ:
Cu(NO3)2 → CuO + NO2 + O2
AgNO3 → Ag + NO2 + O2
Phản ứng oxi hóa khử tự nhiên
Phản ứng này chất khử mà cũng đồng thời là chất oxi hóa
Ví dụ:
Cl2 + 2KOH → KCl + KClO + H2O
4KClO3 → 3KClO4 + KCl

Ý nghĩa của phản ứng oxi hóa khử trong đời sống
Phản ứng oxi hóa khử được coi là một trong những quá trình quan trọng nhất của thiên nhiên: Quá trình hô hấp của thực vật hấp thụ khí cacbonic giải phóng oxi, sự trao đổi chất và hàng loạt quá trình sinh học khác đều có cơ sở dựa trên các phản ứng oxi hóa – khử.
Ngoài ra phản ứng oxi hóa khử còn có ý nghĩa trong nhiều lĩnh vực khác: Sự đốt cháy nhiên liệu trong các động cơ đốt trong. Các quá trình điện phân, phản ứng xảy ra trong pin và trong acquy đều có sự tham gia của phản ứng oxi hóa khử.
Trong lĩnh vực luyện kim, hóa chất, dược phẩm, phân bón hóa học,chất dẻo,… đều cần sự tham gia của các phản ứng oxi hóa – khử.
Bài tập về phản ứng oxi hóa khử

Dưới đây là một số bài tập vận dụng giúp bạn hiểu rõ hơn về phản ứng oxi hóa khử.
Bài 1: Đâu là phản ứng oxi hóa khử trong các phản ứng sau?
- 2HgO → 2Hg + O2
- CaCO3 → CaO + CO2
- 2Al(OH)3 → Al2O3+ 3H2O
- 2NaHCO3 → Na2CO3+ CO2+ H2O
Đáp án A
Sự thay đổi số oxi hóa của các chất trong phản ứng như sau:
Hg2+ + 2e → Hg0
2O2- → O2 + 4e
Bài 2: Cho các phản ứng sau đây, trong phản ứng nào thì NH3 đóng vai trò là chất khử?
- 2NH3 + 3Cl2→ N2+ 6HCl.
- 4NH3+ 5O2→ 4NO + 6H2O.
- 2NH3 + 3CuO → 3Cu + N2+ 3H2O.
- 2NH3 + H2O2 + MnSO4 → MnO2+ (NH4)2SO4.
Đáp án D
Bài 3: Hãy xác định phản ứng nào là phản ứng oxi hóa khử trong các phương trình sau:
- HNO3 + NaOH → NaNO3 + H2O.
- N2O5+ H2O → 2HNO3.
- 2HNO3+ 3H2S → 3S + 2NO + 4H2O.
- 2Fe(OH)3 → Fe2O3+ 3H2O.
Đáp án C
Bài 4: Phản ứng oxi hóa – khử là gì? Cho 3 ví dụ về phản ứng oxi hóa khử.
Câu trả lời: Phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự chuyển đổi electron giữa các chất trong phản ứng.
3 ví dụ về phản ứng oxi hóa khử:
H2 + Cl2 → 2HCl
Cu + 2H2SO4 → CuSO4 + SO2 + 2H2O
Mg + 2HCl → MgCl2 + H2
Bài 5: Cần bao nhiêu gam đồng để khử hoàn toàn lượng ion bạc có trong 85ml dung dịch AgNO3 0,15M.
Lời giải:
Phương trình phản ứng hóa học
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Số mol của AgNO3 là: nAgNO3 = 0.15 x 0.85 = 0.01275 mol
Theo phương trình ta có:
Số mol đồng cần dùng là: nCu = ½ nAgNO3 = 0,01275/2 = 0,006375 mol
Vậy khối lượng đồng cần dùng là: mCu = 0,006375 x 64 = 0,408 gam
Bài 6: Trong phân tử NH4NO3 thì số oxi hóa của 2 nguyên tử nitơ là bao nhiêu?
- -1 và + 1
- -4 và +6
- -3 và + 5
- -3 và +6
Đáp án C
Nitơ trong gốc NH4 có số oxi hóa -3
Nitơ trong gốc NO3 có số oxi hóa +5
Bài 7. Cho quá trình Fe2+ → Fe3+ + 1e. Đây là quá trình gì?
- Oxi hóa
- Khử
- Tự nhận Proton
- Tự oxi hóa khử
Đáp án A
Quá trình oxi hóa là quá trình nhường electron
Bài 8. H2S đóng vai trò gì trong phản ứng oxi hóa khử sau:
2FeCl3 + H2S → 2FeCl2 + S + 2HCl
- Chất oxi hóa
- Chất khử
- Axit
- Vừa là chất oxi hóa vừa là chất khử
Đáp án B
Trên đây là những thông tin về phản ứng oxi hóa khử và một số bài tập áp dụng. Mong rằng qua bài viết này sẽ giúp bạn có được nhiều thông tin hữu ích.