Al hóa trị mấy? Nhôm có những tính chất vật lý và hóa học gì? Bài viết dưới đây sẽ giúp bạn hiểu rõ hơn về kim loại nhôm và những thông tin liên quan nhé.
Al hóa trị mấy?
Al là một kim loại quen thuộc không chỉ trong chương trình học mà còn ở đời sống thường ngày với rất nhiều ứng dụng hữu ích. Bởi vậy, cũng có nhiều câu hỏi xoay quanh kim loại này.

Nhôm (Al) có hóa trị bao nhiêu?
Trả lời: Al có hóa trị 3.
Các thông tin khác về nguyên tố Al
- Nguyên tử khối: 26,982 g/mol (Thường lấy 27 g/mol)
- Số hiệu nguyên tử: Z = 13
- Cấu hình electron: 1s22s22p63s23p1 hay viết gọn lại [Ne]3s23p1
- Thuộc nhóm IIIA, chu kỳ 3
- Al là nguyên tố p và có 3e hoá trị nên Al có xu hướng nhường 3e tạo ion dương Al3+: Al → Al3+ + 3e
- Độ âm điện: 1.61
- Kiểu mạng tinh thể: Lập phương tâm diện.
Tính chất vật lý của nhôm
Dưới đây là các tính chất vật lý của nhôm:
- Trạng thái: Chất rắn.
- Nhôm là kim loại có màu trắng bạc, ánh nhẹ. Nhôm rất nhẹ, dẻo, có thể cán mỏng hoặc kéo thành sợi tùy theo nhu cầu sử dụng.
- Màu sắc: Nhôm có màu trắng bạc, ánh kim nhẹ.
- Nhiệt độ nóng chảy: 660 độ C.
- Khả năng dẫn điện và dẫn nhiệt: Kim loại nhôm có khả năng dẫn điện và dẫn nhiệt rất tốt.

Tính chất hóa học của Al
Nhôm là một kim loại điển hình, vì vậy nó có đầy đủ các tính chất của một kim loại. Cụ thể là:
Tác dụng với phi kim
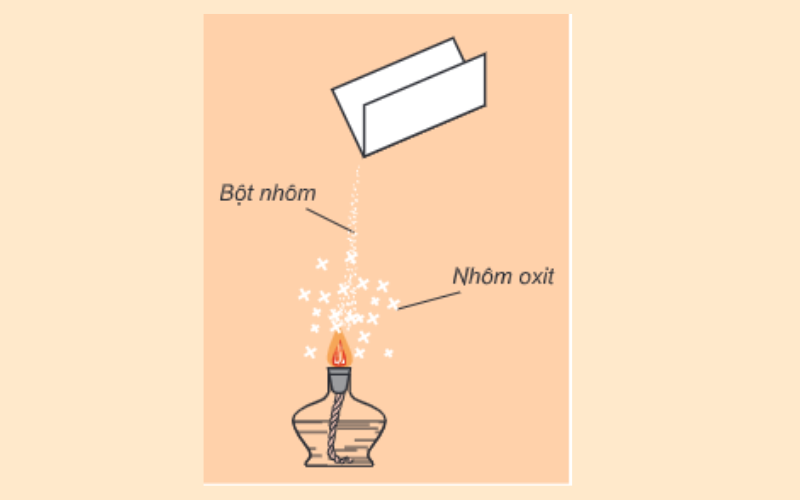
Tác dụng với oxi
Ở nhiệt độ thường tạo lớp màng oxit bảo vệ. Nếu đốt bột nhôm thì phản ứng xảy ra mạnh.
Phương trình hóa học:
4Al + 3O2 → 2Al2O3
Tác dụng với các phi kim khác
Nhôm phản ứng với Cl2, Br2 phản ứng ngay ở nhiệt thường tạo thành muối, phản ứng bốc cháy.
Phương trình hóa học:
2Al + 3Cl2 → 2AlCl3
Khi đun nóng, nhôm phản ứng được với I2, S. Khi ở nhiệt độ cao hơn, nhôm phản ứng được với N2, C.
2Al + 3S → Al2S3
2Al + N2 → 2AlN
2Al + 3C → Al4C3
Tác dụng với axit
Tác dụng với axit thường
Nhôm dễ dàng khử ion H+ thành H2.
2Al + 6HCl → 2AlCl3 + 3H2
Tác dụng với axit mạnh
Nhôm không tác dụng với axit H2SO4, HNO3 đặc nguội. Al tác dụng mạnh với axit HNO3 loãng, H2SO4 đặc, nóng.
Phương trình hóa học:
Al + 4HNO3 → Al(NO3)2 + NO + H2O
2Al + 6H2SO4 đặc, nóng → Al2(SO4)3 + 3SO2 + 6H2O
Tác dụng với oxit kim loại
Phản ứng nhiệt nhôm. Ở nhiệt độ cao, Al khử được nhiều ion kim loại trong oxit (Fe2O3, CuO, Cr2O3,…) thành kim loại tự do.
Phương trình minh họa:
2Al + Fe2O3 → Al2O3 + 2Fe
Tác dụng với nước
Vật dụng làm từ nhôm không tác dụng với H2O ở bất kì nhiệt độ nào nào vì nó có lớp oxit bảo vệ bên ngoài. Tuy nhiên, nếu lớp bảo vệ bị loại bỏ thì nhôm khử được nước ở nhiệt thường. Tuy nhiên, phản ứng này nhanh chóng dừng lại vì tạo ra kết tủa Al(OH)3 bao phủ bên ngoài.
Tác dụng với dung dịch kiềm
Nhôm là một kim loại lưỡng tính nên có thể tác dụng với bazơ.
2Al + 2NaOH + 6H2O → 2Na[(Al(OH)4] + 3H2↑
Không chỉ kim loại nhôm mà các hợp chất của nhôm như Al2O3, Zn(OH)2,…đều là các chất lưỡng tính. Những chất này có thể tác dụng được với axit và bazơ.
Ứng dụng của nhôm
Nhôm là một kim loại rất quen thuộc trong đời sống hàng ngày với rất nhiều ứng dụng.
Ứng dụng nhôm trong công nghiệp
Với đặc tính sáng và không rỉ sét, Al là một vật liệu xuất hiện trong hầu hết mọi nhà máy. Nhiều chi tiết máy móc được chế tạo từ nhôm như khung xe máy, khung xe hơi, thùng xe tải, các chi tiết tản nhiệt cho thiết bị…
Ứng dụng trong ngành hàng không vũ trụ
Al được sử dụng trong sản xuất các chi tiết máy móc trong ngành hàng không vũ trụ như thân và cánh máy bay được làm bằng nhôm. Lý do bởi nhôm có khối lượng riêng nhẹ và bền, rất phù hợp để giảm trọng lượng.
Ứng dụng nhôm trong y tế
Nhôm là một kim loại, nhưng hợp chất alumin có những đặc tính để ứng dụng trong y tế. Với đặc tính mịn của oxit nhôm nên nó được sản xuất bề mặt tiếp xúc của các bộ phận giả trên cơ thể (chân, tay, hông,…) mà vẫn an toàn với sức khỏe. Bên cạnh đó, nhôm oxit còn được sử dụng trong kem che khuyết điểm, phấn, son môi,… nhờ sự mịn, bóng của nó.
Ứng dụng trong xây dựng
Nhiều vật liệu được làm bằng nhôm. Những vật liệu xây dựng phổ biến được làm từ nhôm đó là các loại cửa, tủ nhôm, mái hiên, vách ngăn…
Ứng dụng nhôm trong cuộc sống hàng ngày
Nhôm được dùng làm đồ gia dụng trong nhà như xoong nồi, chảo, tủ quần áo, móc áo, mắc áo, bàn ghế nhôm, giường nhôm,…
Nhờ đặc tính dễ dát mỏng, nhôm cũng là thành phần trong giấy bọc bánh kẹo, thực phẩm để nướng,…

Một số bài tập vận dụng
Bài 1: Phát biểu nào sau đây không đúng về nhôm?
A. Nhôm có khả năng tan được trong dung dịch axit và dung dịch bazơ.
B. Bột nhôm có khả năng tác dụng với H2O ở điều kiện thường,
C. Vật làm bằng nhôm có thể tác dụng với H2O ở nhiệt độ cao.
D. Người ta có thể dùng thùng bằng nhôm để chuyên chở dung dịch HNO3 đặc, nguội và H2SO4 đặc, nguội.
Đáp án C
Bài 2: Cho Dung dịch A chứa Al2(SO4)3, dung dịch B chứa KOH. Cho 150ml hoặc 600ml dung dịch B vào 200ml dung dịch A. Sau phản ứng hoàn toàn, lọc lấy kết tủa, nung đến khối lượng không đổi đều thu được 0,204 gam chất rắn. Nồng độ mol của dung dịch A là:
A. 0,0325.
B. 0,0650.
C. 0,0130.
D. 0,0800.
Đáp án A
Lời giải:
Gọi nồng độ mol của Al2(SO4)3 và KOH lần lượt là a và b
Trường hợp 1: 150ml dung dịch B vào 200ml dung dịch A, KOH hết, Al2(SO4)3 dư
nOH- = 3nAl(OH)3 = 6nAl2O3
Trường hợp 2: 600ml dung dịch B vào 200 ml dung dịch A, Al2(SO4)3 phản ứng hết tạo kết tủa, kết tủa này tan một phần trong KOH dư
nOH- = 4nAl3+ – nAl(OH)3
Hay: 8.0,2a – 2.2.10-3 0,048
a = 0,0325 M
Bài 3: Cho 2 phương trình phản ứng sau:
(1) 2Al + 6HCl → 2AlCl3 + 3H2
(2) 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
Kết luận nào sau đây không đúng?
A. Nhôm khử được ion H+ của axit trong dung dịch axit.
B. Nhôm phản ứng được với dung dịch kiềm.
C. Nhôm phản ứng với cả dung dịch axit và dung dịch kiềm nên nhôm là chất lưỡng tính.
D. Nhôm là kim loại có tính khử mạnh. Trong cả 2 phản ứng này, Al đều bị oxi hóa thành ion dương.
Đáp án B
Bài 4: Tại sao phèn chua có tác dụng làm trong nước ?
A. Phèn chua chứa các ion K+, Al3+, SO42- có thể hấp phụ các chất lơ lửng trong nước.
B. Phèn chua phản ứng với các chất bẩn thành các chất tan trong nước.
C. Khi hòa tan trong nước, phèn chua thủy phân ra ion H+, ion này hấp phụ rất tốt các chất lơ lửng trong nước.
D. Khi hòa tan trong nước, phèn chua thủy phân ra Al(OH)3. Al(OH)3 với bề mặt phát triển, hấp phụ các chất lơ lửng trong nước, kéo chúng cùng lắng xuống dưới.
Đáp án D
Bài 5: Khi cho từ từ dung dịch HCl đến dư vào dung dịch Na[Al(OH)4] thì có hiện tượng gì xảy ra?
A. Ban đầu xuất hiện kết tủa keo trắng, sau một thời gian kết tủa tan dần.
B. Có kết tủa keo trắng.
C. Ban đầu không có hiện tượng gì, sau một thời gian xuất hiện kết tủa keo trắng.
D. Không có hiện tượng gì xảy ra.
Đáp án A
Lời giải:
Khi cho dung dịch HCl dư vào dung dịch Na[Al(OH)4] ta có các phương trình phản ứng như sau:
HCl + Na[Al(OH)4] → NaCl + Al(OH)3↓ + H2O
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Ban đầu xuất hiện kết tủa keo trắng là Al(OH)3 sau một thời gian kết tủa tan dần do phản ứng tiếp với HCl dư.
Trên đây là đáp án cho câu hỏi “Al hóa trị mấy?” và các thông tin liên quan. Mong rằng bài viết sẽ giúp bạn có thêm được những kiến thức hữu ích.